Патокинез острых нарушений мозгового кровообращения (ОНМК)
Патокинез острых нарушений мозгового кровообращения (ОНМК), включая все многообразие факторов этиологии и патогенеза сосудистых заболеваний мозга, условия и причины инсульта, последовательность развития патологических процессов, сопутствующих цереброваскулярной недостаточности, предполагает необходимость оценки финальных изменений гемодинамики, непосредственно связанных с мозговой катастрофой.
Для каждого больного характерен свой путь накопления последовательно и параллельно протекающих патологических процессов, создающих «критическую массу» органических и функциональных нарушений, которые под воздействием факторов дестабилизации, однажды, приводят к возникновению лавинообразно нарастающих сдвигов, затрагивающих всю систему кровообращения - гемодинамическому кризу. Эксплозивное развитие криза обусловлено каскадом взаимосвязанных патофизиологических процессов, в которые вовлекаются все составляющие треугольника «сердце-сосуды-кровь», что приводят к ярким клиническим проявлениям недостаточности системного и (или) регионального кровообращения.
Для большинства хронических заболеваний сердечно-сосудистой системы характерно длительное течение с периодами обострений. Но в некоторых случаях, такое обострение носит характер обвала, криза (crisis - фр. - внезапная перемена в течении болезни). Криз отличается от обострения болезни двумя важнейшими признаками: скоротечностью развития событий и декомпенсацией кровообращения, которая проявляется как на уровне как центральной, так и региональной гемодинамики.
Клиницисты всегда отделяли криз от обострения болезни. Термин «гипертонический криз» ввел австрийский врач P. Jacob (1903г.). Он выделял общие и местные сосудистые кризы и считал, что в их основе лежит внезапно возникающее повышение АД, связанное со спастическим сокращением сосудов. В 1951 г. D.Brown впервые использует понятие «церебральные гемодинамические кризы» для описания внезапных нарушений мозгового кровообращения при развитии вазоспастических реакций. А.Л.Мясников (1954) различал гипертонические кризы с общей вегетативно-сосудистой симптоматикой, и кризы, протекающие с нарушением кровообращения мозга, сердца, почек.
Изучению патогенеза и клинических проявлений сосудистых кризов были посвящены фундаментальные работы Н.К.Боголепова, Е.В.Шмидта и других выдающихся отечественных неврологов. В последние годы многочисленные публикации авторитетных клиницистов (Е.Е.Гогин, А.П.Голиков, С.Г.Моисеев, М.С. Кушаковский, Н.А. Ратнер, И.В.Шхвацабая, и др) содержали результаты исследования различных аспектов патогенеза и клинических проявлений гипертонического криза.
Наблюдательные исследователи в развитии гипертонического криза отмечали самое главное - не просто повышение АД выше привычного для данного пациента уровня, но сочетание гипертонии с нарушениями местной перфузии тканей в каком-либо жизненно важном русле [1,2].
Таким образом, в результате многолетних наблюдений, сложились представления о клинических проявлениях, по крайней мере, двух патогенетических вариантов гемодинамических (сосудистых) кризов: гипертонического (который, безусловно, связан с повышением АД) и церебрального (который так же связан с быстротечными сосудистыми реакциями, но не обязательно с повышением АД). Термин «гемодинамический криз», очевидно, шире, чем «сосудистый» или гипертонический криз. Ведь криз, по своим пусковым механизмам, может быть и не совсем «сосудистым», а в большей степени «сердечным» (например, пароксизм мерцательной аритмии).
Предположив, что инсульт всегда является результатом декомпенсации кровообращения на каком-либо уровне, представляется вполне обоснованным установить связь между гемодинамическими кризами и ОНМК. Однако, для этого необходимо выделить патогенетические варианты гемодинамических кризов и определить критерии их диагностики.
Тщательное изучение анамнеза и обстоятельств мозговой катастрофы в большинстве случаев позволяет установить не только традиционные факторы риска, но и характер гемодинамического криза, завершившегося инсультом и факторы дестабилизации мозгового кровообращения. Врачам хорошо известно, что в большинстве случаев ОНМК ассоциируются с гипертоническим кризом [3-6]. Развитию очаговой неврологической симптоматики нередко предшествуют пароксизмальные нарушения ритма сердца. Реже удается установить связь инсульта с коронарным синдромом (хотя клинические варианты такого криза описаны еще Н.К.Боголеповым). Другие сосудистые эпизоды (артериальная гипотония, нейроэндокринные нарушения) в некоторых случаях принимают очевидное участие в патогенезе заболевания, но маскируются завесой гипертонии и атеросклероза.
Для эффективного функционирования современной системы индивидуальной профилактики инсульта необходимо знать характер возможного гемодинамического криза «до», а не «после» разрушения мозга.
Современные методы кардионеврологического обследования уверенно обнаруживают признаки, которые могут служить предикторами гемодинамического криза. Репрезентативные синдромы представляют врачу механизмы возможной декомпенсации кровообращения, а факторы дестабилизации и факторы риска указывают вероятный путь ее проявления. Правильная и своевременная оценка гемодинамических и гемостатических резервов позволяет врачу обнаружить «тонкое звено» в патогенетической цепи, связывающей патологические процессы, приводящие к инсульту.
Анализ клинических, анамнестических, лабораторных и инструментальных данных определяет возможность выделять и клинически идентифицировать несколько патогенетических вариантов гемодинамических кризов:
- гипертонический
- гипотонический
- гипотонический
- аритмический
- нейроэндокринный
- ангиодистонический
- гемореологический
- обтурационный
Наши многолетние наблюдения, позволяют утверждать, что восемь патогенетических вариантов гемодинамических кризов в полной мере ассоциируются с непосредственными причинами ОНМК [7,8].
Если в некоторых случаях, инсульт не удается связать с каким-либо гемодинамическим кризом, то это результат недостатка анамнестических данных или ограниченного объема кардионеврологического обследования.
Гипертонический криз
Гипертонический криз - одна из наиболее частых причин развития гемодинамического варианта ишемического инсульта.
С гипертоническим кризом связано абсолютное большинство ОНМК. Наклонность к гипертоническим кризам закономерно ведет к очаговым повреждениям мозга в результате лакунарных инфарктов или гемодинамических инсультов [9].
Не уменьшающееся число гипертонических кризов является одной из существенных причин высокой заболеваемости инсультом. По данным Национального научно-практического общества скорой медицинской помощи, в целом по России только в течение последних лет 20 века число вызовов бригад по поводу гипертонического криза и связанная с этими обстоятельствами госпитализация увеличилась в 1,5 раза. Гипертонические кризы составляют около 20% всех причин вызова бригады скорой помощи и 30% всех состояний, требующих неотложной помощи [4,5].
Существует множество классификаций гипертонических кризов - Н.А.Ратнер (1958), Моисеев С.Г. (1976), Кушаковский М.С. (1977), Голиков А.П. (1976,1985), Барт Б.Я.(1995). На 5-м съезде Всероссийской ассоциации по изучению артериальной гипертонии им. Г.Ф.Ланга-А.Л.Мясникова (1998) предложена одна из наиболее приближенных к практическим целям классификаций гипертонических кризов.
Классификация гипертонических кризов
А. По предполагаемому патогенезу:
-
Первичные - при наличии эссенциальной АГ
-
Вторичные - приналичии заболевания, при котором АГ может быть вторичной (феохромоцитома, альдостерома, тиреотоксикоз,токсикоз беременных, заболевания почек, мозга и его оболочек, коарктация аорты и др).
В. По основным клиническим проявлениям:
1. Церебральные.
2. Кардиальные: ишемические, аритмические, с левожелудочковой недостаточностью.
3. С возможным поражением аорты (расслоение).
4. С поражением структур глаза.
5. С поражением почек.
6. С вегетативными проявлениями.
По-видимому, все многообразие клинических проявлений гипертонических кризов обусловлено индивидуальными особенностями и характером заболеваний пациента, состоянием гемодинамических и гемостатических резервов. Поэтому даже у одного больного кризы могут протекать по-разному. Частота и клинические проявления гипертонических кризов в значительной мере зависят от возраста. По данным И.Н.Бондаревой (2004 г.) на возрастную группу от 40 до 59 лет приходится 63% всех кризов, ОНМК осложняются 2% гипертонических кризов, а в 11% наблюдений криз был первым проявлением гипертонической болезни. У больных старше 60 кризы протекают тяжелее, чаще приводят к развитию церебральных и кардиальных синдромов [9].
Отсутствие практики постоянного лечения гипертонической болезни, злоупотребление алкоголем, заболевания почек, нейроэндокринные нарушения - наиболее частые причины внезапного повышения АД и «запуска» механизмов декомпенсации кровообращения [9-12].
Анализ наших собственных наблюдений, основанный на изучении анамнестических данных о 100 больных, перенесших гипертонический криз, свидетельствует, что большинство опрошенных, связывает внезапное повышение АД и связанные с этим осложнения со стрессом (Табл. 1).
Таблица 1
Связь гипертонического криза с факторами дестабилизации

Обращает на себя внимание, крайне незначительное число факторов, с которыми пациенты связывают развитие гемодинамического криза, и среди этих факторов второе место занимает употребление алкоголя.
Разнообразие клинических проявлений гипертонических кризов во многом определяется состоянием гемодинамических резервов. Внезапное повышение АД, сопровождается спазмом периферических артерий, увеличением периферического сопротивления и нагрузки на миокард. Безболевая ишемия миокарда обнаруживается у 42% больных с гипертоническими кризами в первые сутки и у 14% - на пятые сутки [11]. Срыву компенсации системы кровообращения при гипертоническом кризу способствует закономерная смена гиперкинетического типа кровообращения на гипокинетический, что отражает нарушение функции гипертрофированного миокарда [12]. В период криза, преходящие нарушения локальной сократимости миокарда обнаруживаются у 70 - 90% больных [8,12,13]. Система кровообращения, находящаяся в состоянии напряженной гиперфункции проявляет признаки декомпенсации, что проявляется кратковременным снижением ударного и минутного объема крови.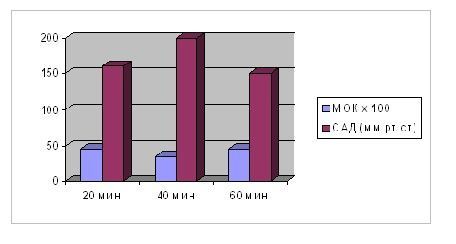
Рис. 1. Минутный объем крови (МОК) и систолическое АД (САД) в период гипертонического криза
В 1995 году при ретроспективном анализе показателей центральной гемодинамики больных, перенесших ишемический инсульт, нам удалось показать, что в течение нескольких лет, предшествовавших мозговой катастрофе, у большинства больных нарастали скрытые признаки сердечной недостаточности [8].
Снижение фракции выброса и минутного объема крови (кардиальный гиподинамический синдром) у больных с гипертонической болезнью является доклиническим признаком снижения кардиального гемодинамического резерва. Критическое повышение периферического сопротивления сосудистого русла в период развития гипертонического криза приводит к снижению МОК и ишемии мозга.
С гипертоническим кризом чаще патогенетически связаны лакунарный и гемодинамический инсульт, однако сложные, стремительно протекающие системные нарушения не исключают развития и других подтипов ишемического инсульта: атеротромботического, артерио- или кардиоэмболического.
Гипотонический криз
Гипотонический криз в действительности становится причиной инсульта чаще, чем это принято считать. Только в последние годы, с внедрением в клиническую практику методов мониторирования АД, исследователи стали обращать внимание на периодическую относительную гипотензию у больных, адаптированных к высоким цифрам АД [5,14-18]. По данным НИИ неврологии не менее 21% ОНМК происходит на фоне значительного снижения АД, вызванного неадекватным использованием антигипертензивных препаратов. Эпизодическая артериальная гипотензия характерна для больных с тяжелыми атеросклеротическими поражениями брахиоцефальных артерий. «Конституциональные гипотоники» при определенных условиях, при действии факторов дестабилизации, способны демонстрировать гипотонические кризы с пароксизмальными нарушениями сознания (преходящие нарушения мозгового кровообращения), а в некоторых случаях и очаговыми повреждениями мозга [15]. Гипотонические кризы характерны для больных паркинсонизмом с проявлениями выраженной вегетативной дисфункции. Гипотонические эпизоды являются одной из причин диффузного повреждения мозга и «ночных» инсультов. Казалось бы, кратковременные периоды снижения АД, не могут иметь самостоятельного значения в патогенезе ОНМК. Но артериальная гипотензия служит таким же пусковым механизмом, для развертывания каскадных коагулопатических и гемодинамических реакций, которые включают развитие взаимоотягощающих патологических процессов. Не случайно, через некоторое время после критического падения АД, когда пациент попадает в поле зрения врачей, клинические проявления этого варианта гемодинамического криза уже определяются «рикошетными» синдромами - артериальной гипертонией, гиперкоагуляцией, коронарной и церебральной ишемией, отеком мозга.
Наиболее вероятными факторами дестабилизации для гипотонических кризов следует считать агрессивные методы лекарственной терапии, интоксикации, обострения заболеваний, протекающих с нарушением центральной или сегментарной вегетативной регуляции кровообращения.
Коронарный криз
Коронарный криз может быть непосредственно связан с развитием церебральной ишемии в силу общности патогенеза ишемической болезни сердца и мозга. В некоторых случаях эта связь представляется очевидной, и проявления цереброваскулярной недостаточности сопутствуют приступам стенокардии [1,19]. Но чаще скрытая коронарная недостаточность включает каскад гемодинамических и гемостатических сдвигов, заканчивающихся инсультом. По данным А.В.Фонякина (2005) более чем у 16% больных с гемодинамическим инсультом при холтеровском мониторировании выявлены транзиторные эпизоды безболевой ишемии миокарда (БИМ). Продолжительность ишемии варьировала от 10 до 90 мин. Патогенетическое значение коронарной недостаточности в развитии церебральной ишемии заключается в возможности транзиторных нарушений сократимости миокарда [20]. Это обстоятельство оказывается весьма значимым для больных с субкомпенсированной церебральной гемодинамикой и низкими гемодинамическими резервами. БИМ в некоторых случаях проявляется компенсаторным увеличением частоты сердечных сокращений и ухудшением диастолической функции миокарда. В конечном счете, явная и скрытая коронарная недостаточность приводит к снижению МОК (и) или АД.
Риск ОНМК при коронарном синдроме связан с кардиогенной эмболией или относительной недостаточностью кровоснабжения головного мозга при критическом снижении МОК. Коронарный криз является относительно редкой причиной инсульта (в сравнении с другими патогенетическими варианта гемодинамических кризов). В базе данных международного регистра The Global Registry of Acute Coronary Events (GRACE) есть сведения о 35 233 пациентах с верифицированным коронарным синдромом (37% - инфаркт миокарда с подъемом сегмента ST, 30% - без подъема ST, 33% - больные с нестабильной стенокардией). Инсульт в течение ближайших 6 месяцев после коронарного эпизода развился у 1,6% больных. Тем не менее, острый коронарный эпизод, при определенных обстоятельствах (выраженные атеросклеротические изменения магистральных артерий головного мозга, микроциркуляторные нарушения, макро- и микроангиопатия), способен инициировать каскадные патофизиологические реакции, протекающие с нарушением системного и регионального кровообращения - гемодинамический криз.
К коронарному кризу чаще приводит стресс, избыточная физическая нагрузка и другие факторы дестабилизации, способствующие активации атеросклероза и внутрисосудистому тромбообразованию.
Аритмический криз
Аритмический криз – острое нарушение системной и региональной гемодинамики, возникающее вследствие пароксизмальных или постоянных нарушений ритма сердца. Это одна из основных причин кардиоэмболического и гемодинамического инсульта. В ряде случаев единственным проявлением нарушений ритма могут быть транзиторные ишемические атаки (ТИА) или синкопальные состояния. Не менее 20% ОНМК обусловлено кардиогенной эмболией, обусловленной аритмией [14,19]. Гемодинамический механизм церебральной ишемии при аритмических кризах играет меньшую роль, но необходимо учитывать, что пароксизм фибрилляции предсердий снижает МОК примерно на 20 - 25%. При желудочковых формах аритмий гемодинамические нарушения еще более выражены [20-23]. При выраженных атеросклеротических изменениях магистральных артерий такое снижение эффективной работы сердца существенно сказывается на состоянии церебральной гемодинамики [8,17].
Установлено, что синдром слабости синусового узла встречается значительно чаще у пациентов с ТИА и инсультами неясной этиологии [23]. Дисфункция синусового узла может проявляться синусовой брадикардией, синоатриовентрикулярной блокадой, эпизодами асистолии. У 40-50% больных с дисфункцией синусового узла отмечается так называемая хронотропная недостаточность – неспособность к адекватному ускорению частоты сердечных сокращений под влиянием физиологических стимулов [24].
Пароксизмальные формы аритмий редко диагностируются своевременно и это оказывает влияние на статистические данные, получаемые при выполнении крупных исследований. Бессимптомные формы аритмий встречаются чаще симптомных, а холтеровское мониторирование не входит в скрининговый объем исследований больших категорий больных. По данным А.В.Фонякина (2005) у 48% пациентов с инсультом пароксизмы аритмии протекали бессимптомно. По результатам холтеровского мониторирования асимптомные эпизоды мерцания предсердий превышают симптомные в 12 и более раз. Фибрилляция предсердий обнаруживается случайно у 14-25% пациентов с ИИ [25,26]. Внезапная смерть (19 до 159 случаев на 100000 населения в год) в значительной степени связана с фатальными нарушениями ритма сердца [27,28].
Нейроэндокринный криз
Нейроэндокринный криз развивается вследствие дезорганизации нейрогормональной регуляции гемодинамики. К тяжелым и опасным гемодинамическим кризам приводят дисгормональные нарушения, сопутствующие гормональноактивным новообразованиям. ОНМК являются типичным осложнением, а часто и первым клиническим проявлением феохромоцитомы [29].
Внезапные массивные выбросы в кровь катехоламинов определяют кризовое течение заболевания. Повреждающее действие гормонально-активной опухоли не ограничивается кризовым повышением АД. В патогенезе ОНМК значительную роль играет спазм периферических артерий и токсическое влияние катехоламинов на сосудистую стенку и миокард. Миокардиодистрофия, ангиопатия, гиперкоагуляция и вазоспазм в полной мере заменяют, характерные для пожилых «атеросклеротические» условия для возникновения инсульта. Артериальная гипертония наблюдается у 76 – 100% больных с выявленными феохромоцитомами [30]. Избыточное поступление в кровь катехоламинов увеличивает частоту сердечных сокращений, системный сосудистый тонус. При феохромоцитоме формируется гиперкинетическая, сосудосуживающая, гиповолемическая форма артериальной гипертензии [8,29]. В формировании АГ у больных с феохромоцитомой важное значение имеют не только катехоламины. Установлено влиняие дезоксикортикостерона и депрессорных простагландинов [31]. Стандартная физическая нагрузка выявляет снижение функциональных резервов миокарда у всех больных [32]. Влияние избыточной секреции катехоламинов приводит и к другим изменениям – повышению концентрации глюкозы в крови, а следовательно и повышению вязкости плазмы. Результатом хронического катехоламинового стресса может быть стать кардиомиопатия со стойкими нарушениями ритма сердца и сердечной недостаточностью.
Клиническая значимость гиперкатехоламинемии иллюстрируется нейроэндокринным кризом, который возникает при пальпации опухоли. Патогенез гемодинамических расстройств при нейроэндокринных опухолях сложен и не может быть сведен только к повышению АД, хотя в типичных случаях выявляется прямая зависимость между величиной АД и экскрецией норадреналина. Норадреналин - основной медиатор симпатической нервной системы. Норадренергические нейроны обнаруживаются в среднем мозге, в области варолиева моста, продолговатом и промежуточном мозге. Это во многом объясняет наличие ярких вегетативно-эмоциональных нарушений у больных с гормонально-активными опухолями. Они сходны с гипоталамическими прессорными реакциями: тахикардия, расширение зрачков, полиурия, пилоэрекция и другие проявления вегетативной дисфункции. Как правило, гипоталамический синдром трудно выделить из общей картины заболевания. Именно это обстоятельство – системность патологического процесса с участием нарушений центральной и региональной гемодинамики, гемостаза, вегетативной дисфункции – отличает нейроэндокринный криз от простого повышения АД.
Нарушения гемодинамики при нейроэндокринных опухолях не ограничиваются феохромоцитомой. Для карциноидного синдрома характерны нарушения метаболизма триптофана, серотонина, гистамина [29]. Дисфункция серотонинэргической системы приводи к развитию комплекса нейроэндокринных расстройств, которые носят пермонентный и приступообразный характер. Выброс серотонина сопровождается повышением АД, брадикардией, бронхоспазмом. Под действие серотонина возникает сосудистый спазм. Гистамин, кинины, полипептидные гормоны, выделяемые карциноидом, способны вызывать разноообразные эффекты гемодинамической нестабильности, которые могут стать непосредственной причиной инсульта у больных с низкими гемодинамическими резервами.
Нейрогормональная дисфункция характерна для женщин в климактерическом периоде. Неустойчивость АД, ангиодистонические реакции, эмоциональная лабильность – хорошо известные клиницистам признаки снижения адаптационных возможностей, предрасполагающих к кардиальным и церебральным сосудистым событиям. В целом, женщины меньше подвержены ОНМК, чем мужчины, однако эта закономерность нивелируется в старших возрастных группах, в после 80 лет инсульт чаще встречается у женщин. Протективная роль эстрогенов в полной мере проявляет себя только в продуктивном возрасте [33]. Считается, что заместительная гормональная терапия улучшает эндотелиальную функцию, липидный обмен и, в целом, снижает риск атеросклероза. Однако, прием синтетический гормонов увеличивает прокоагуляционные свойства крови и в целом протективный эффект оказывается недостаточным.
Нейроэндокринный криз чаще приводит к гемодинамическому механизму ишемического повреждения головного мозга.
Ангиодистонический криз
Ангиодистонический криз характерен для вертеброгенных нарушений сосудистого тонуса. При нарушениях мозгового кровообращения, обусловленных вертеброгенными влияниями дисциркуляция, в системе позвоночных артерий определяет основные клинические проявления. И хотя до 70% всех ОНМК в системе позвоночных артерий составляют транзиторные ишемические атаки с хорошим функциональным выходом, стволовые инсульты могут быть более опасны, чем нарушения гемодинамики в каротидном бассейне. Анатомической основой для веретеброгенных нарушений церебральной гемодинамики могут стать аномалии развития и строения краниовертебрального стыка, посттравматические изменения шейного отдела позвоночника. В рамках вертеброгенных влияний на центральну и церебральную гемодинамику выделяют действие многочисленных факторов (мышечно-тонического, вегетативно-сосудистого, ирритативно-компрессионного и других), клиническая идентификация которых зачастую весьма затруднительна [34]. Принципиально важно, что патологические процессы, нарушения статики позвоночника в шейном и грудном отделах приводят к нарушению регуляции сосудистого тонуса, сердечной деятельности и эти влияния верифицированы современными методами исследования (допплерография, холетровское мониторирование ЭГК, МРТ) [34,35].
Вторичные ишемические повреждения головного мозга, возникающие при внутричерепных кровоизлияниях, являются следствием сосудистого спазма [36]. В некоторых случаях ишемический инсульт после субарахноидального кровоизлияния определяет исходы заболевания и тяжесть состояния больных. Ангиодистония - непременный спутник и ведущий патогенетический механизм мигрени. Распространенность заболевания в популяции велика: от 3 до 12% населения подвержены мигрени, в США более 10 млн визитов к врачу в течение года связаны с мигренью [37]. Известно, что на высоте мигренозного приступа нередки очаговые неврологические симптомы: гипестезии, парезы (гемиплегическая мигрень), нарушения зрения. Мигренозный статус – серия тяжелых приступов, продолжающихся несколько дней – приводит к появлению общемозговых и очаговых симптомов. Методы нейровизуализации обнаруживают ишемические очаги, преимущественно в белом веществе головного мозга. Мигренозный инсульт – результат тяжелого течения мигрени, по своим последствиям не отличается от других вариантов гемодинамического инсульта [37,38].
Ангиодистонический криз приводит к развитию гемодинамического инсульта. Локализация ишемических очагов зависит от источника ангиодистонии. Вертеброгенные синдромы чаще приводят к дисциркуляции в системе позвоночных артерий, генерализованный церебральный вазоспазм – к полушарным повреждениям.
Гемореологический криз
Гемореологический криз может служить непосредственной причиной инсульта в тех случаях, когда у больного нет очевидных заболеваний, ассоциированных с ОНМК (АГ, церебральный атеросклероз, аритмия). Гиперкоагуляция и гипервискозность крови служат основой для системных нарушений микроциркуляции, которые при воздействии факторов дестабилизации (гипертермия, обезвоживание, интоксикация, стресс) могут привести к ишемии – ОНМК по типу гемореологической микроокклюзии (гемореологический инсульт). Наиболее распространенным механизмом блокады микроциркуляторного звена кровообращения является внутрисосудистое тромбообразование. Однако, патогенез гемореологического криза сложен и не ограничивается внутрисосудистым гиперкоагуляцией [39,40]. Дислипидемия и гипергликемия приводят к сложным и до конца не ясным изменениям микрососудистого русла (ангиопатия), которые в сочетании с гипервискозностью плазмы крови оказывают существенное влияние на состояние микроциркуляции. Диабет не только ускоряет атерогенез, он патогенетически связан с дислипидемией. У больных сахарным диабетом 2 типа увеличивается концентрация в крови системных прокоагулянтных факторов, повышается содержание фибриногена, снижается фибринолитическая активность крови [40]. Существенное значение в формировании микроциркуляторных нарушений играет полицитемия. Эритремия – наиболее значимый фактор блокады микроциркуляции, который чаще обнаруживает свое патогенное влияние у курящих мужчин. Полицитемия может служить причиной гемореологического криза у больных с заболеваниями крови [41].
Все эти обстоятельства позволяют считать, что гемореологический криз может осложнить течение сахарного диабета, он более вероятен для больных с дислипидемией, многоуровневыми обменные нарушениями (метаболический синдром).
Гемореологический криз имеет все основные черты гемодинамического криза. Региональная ишемия, возникающая вследствие блокады микроциркуляции, приводит к системным гемодинамическим реакциям (артериальная гипертония), генерализованной гиперкоагуляции с реализацией церебрального или коронарного синдрома ишемического повреждения.
Обтурационный криз
Обтурационный криз возникает вследствие закупорки артерии среднего или крупного калибра. Существует несколько патофизиологических механизмов острой обтурации артерии. Наиболее вероятна закупорка сосуда тромбом (атеротромботический и кардиоэмболический инсульт) или фрагментом распадающейся атеросклеротической бляшки. Блокада кровотока «активированной» вследствие кровоизлияния или воспаления атеросклеротической бляшкой, более редкий, но возможный механизм обтурационного криза. Расслаивание стенки артериального ствола так же может стать причиной обтурационного криза [42]. Как правило, закупорка крупной артерии возникает в местах наиболее выраженных артеросклеротических изменений – морфологическая деструкция сосудистой стенки способствует тромбообразованию или расслоению под влиянием факторов дестабилизации. Спонтанная и связанная с травмой диссекция крупных артерий может стать причиной инфаркта головного мозга у молодых в 10 – 25% случаев [43-46]. Рыхлые, гетерогенные бляшки, атеросклеротические стенозы и окклюзии брахиоцефальных артерий, создают наиболее благоприятные условия для обтурационного криза. Острая церебральная ишемия, вызванная нарушениями региональной гемодинамики, неизбежно приводит к развитию системных гемодинамических и дизрегуляторных ответов, гиперкоагуляции – признаков, характеризующих все патогенетические варианты гемодинамических кризов.
Патофизиология гемодинамических кризов
Таким образом, все варианты гемодинамических кризов имеют общие черты – нарушения региональной и системной гемодинамики, срыв регуляторных механизмов компенсации, гиперкоагуляция и микроциркуляторный блок.
Патофизиологию гемодинамических кризов можно представить в виде схемы (Рис.2)
Рис. 2. Патофизиология гемодинамических кризов
Независимо от инициирующих механизмов (нестабильность показателей центральной гемодинамики, микроциркуляторный блок, обтурация артерии) в развитии любого патогенетического варианта гемодинамического криза принимают участие взаимосвязанные патологические процессы, взаимное отягощение которых и определяет стремительное, лавинообразное проявление клинических симптомов. Необходимо отметить, что артериальная гипертония может стать «пусковым» механизмом криза или его вторичным звеном. По-видимому, с этим обстоятельством связано значительное преобладание «гипертонических» кризов, среди причин ОНМК. Кризовое течение гипертонической болезни изменяет проницаемость гематоэнцефалического барьера и оказывает существенное влияние на обмен нейропептидов - регуляторов апоптоза. Специальные исследования продемонстрировали участие иммунных механизмов повреждения в патогенезе дисциркуляторной энцефалопатии, формирующейся у больных с гипертоническими кризами [47].
По нашим наблюдениям с гипертоническим кризом можно связать 40 – 45% ОНМК. Аритмический криз приводит к инсульту в 20-22% наблюдений. Гипотонический криз стал причиной заболевания у 5% больных. Около 10% ОНМК не удается связать с каким-либо вариантом гемодинамического криза. Эти ориентировочные данные основаны, главным образом, на анамнестических сведениях и нуждаются в уточнении с помощью специальных исследований.
Концепция гемодинамических кризов необходима в современной системе профилактики инсульта, потому, что она впервые связывает ОНМК с их причинами.
Предположения о характере возможного гемодинамического криза, базирующиеся на диагностике репрезентативных синдромов, определяют, в конечном счете, индивидуальную превентивную программу. Ведь предупреждение гемодинамического криза = предупреждению инсульта, поскольку без гемодинамического криза, даже при наличии длительно существующих патологических процессов, представленных репрезентативными синдромами, острых нарушений мозгового кровообращения не бывает.
Литература
1. Боголепов Н.К. Церебральные кризы и инсульты. М.1975. – 230 с.
2. Гогин Е.Е. Гипертоническая болезнь. // -М.: 1997. – 400 с.
3. Зонис Б.Я. Амбулаторное лечение гипертонических кризов//ТОПмедицина. – 2001.-№ 1.- С. 16-18.
4. Бокарев И.Н. Гипертонические кризы//Клиническая медицина.-2005.-8; 84-86.
5. Моисеев В.С., Кобалава Ж.Д. АРГУС. Артериальная гипертония у лиц старших возрастных групп. Монография. –М.: «Медицинское информационное агентство», 2002. - 448 с.
6. Арабидзе Г.Г., Белоусов Ю.Б., Карпов Ю.А. Артериальная гипертония (справочное руководство по диагностике и лечению). //-М.: 1999. – 140 с.
7. Симоненко В.Б., Широков Е.А. Роль гемодинамических кризов в этиологии и патогенезе нарушений мозгового кровообращения//ТОП медицина. – 2001. -№10. – С.14-15.
8. Симоненко В.Б., Широков Е.А. Основы кардионеврологии. Издание 2 переработанное и дополненное. -М.: Медицина, 2001. – 239 с.
9. Очерки ангионеврологии/Под редакцией Суслиной З.А. – М.: Из-во «Атмосфера», 2005. – 368 с.
10. Голиков А.П. Терапия гипертонических кризов при гипертонической (эссенциальной) болезни//ТОПмедицина. – 2001.-№ 1.- С. –18-21.
11. Голиков А.П., Лукьянов М.М. Монитогинг ЭКГ при купировании гипертонических кризов//ТОПмедицина. – 2001.-№ 2. - С. 8 -9.
12. Корнева В.А., Петровский В.И., Дуданов И.П. Геометрия миокарда левого желудочка при артериальной гипертонии на фоне стенозирующего церебрального атеросклероза//Клиническая медицина. 2006; 3: 28-31.
13. Жаров Е.И., Сидоренко Б.А., Верткин А.Л. и др. Клиническая оценка преходящей ишемии миокарда. // Кардиология. –1990. –N7. – С.38-43.
14. Sandercock P.A.G., Warrlow C.P., Jones L.N., Starkey I.R. Predisposing factors for cerebral infarction: the Oxford Community Stroke Project. BMJ 1989; 298: 75-80.
15. Чефранова Ж.Ю. Идиопатическая артериальная гипотензия: клиника, диагностика, лечение: Автореф..дисс…д.м.н., Москва, 2004. – 39 с.
16. Машин В.В., Белова Л.А. с соавт. Суточный профиль артериального давления при различных подтипах ишемического инсульта// Артериальная гипертония: органные поражения и сопутствующие заболевания, Ярославль, 2004. – С. 95-96.
17. Rothwell P.M., Slattery J., Warlow C.P. Clinical and angiographic predictors of stroke and death due to carotid endarterectomy; systematic rewiew. BMJ 1997; 315: 1571-1577.
18. Staessen J.A., Wang J. Blood-pressure lowering for the secondary prevention of stroke. Lancet 2001; 358:1026-1027.
19. Budaj A., Frasinska K., Gore J.M. et al. Stroke and coronary syndrom.-Circulation 2005; 111:3242-3247.
20. Верткин А.Л., Мартынов И.В., Гасилин В.С. с соавт. Безболевая ишемия миокарда. Москва, 1995.
21. Ведерникова Ю.П., Вихерт А.М. Функция эндотелия и спазм коронарных артерий // Бюл. ВКНЦ АМН СССР. –N2. -С.13-19.
22. Фонякин А.В., Суслина З.А., Гераскина Л.А. Кардиологическая диагностика при ишемическом инсульте. С.-Пб.: ИНКАРТ, 2005. – 224 с.
23. Abdon N.J., Zettervall O., Carlson J., et al. Is occult atrial disoder a frequent cause of non-hemmoragic stroke? Long-term ECG in 86 patients//Stroke 1982;13:832-837.
24. Джанашия П.Х., Шевченко Н.М., Джанашия Н.Д. Синдром слабости синусового узла//Сердце 2002; 2:97-99.
25. Johnston DC, Hill MD. The patient with transient cerebral ischemia: a golden opportunity for stroke prevention// CMAJ. 2004 Mar 30;170 (7):1134-7.
26. Vinderhoets F., Bogousslavski J., Regli F. Atrial fibrillation after acute stroke//Stroke 1993; 24:26-30.
27. Bogousslavsky J., Regli F. Unilateral watershed cerebral infarcts//Neurology 1986; 36:373-377.
28. Corday E., Irving D.W. Effect of cardiac arrhythmias on the cerebral circulation//Am J Cardiol 1960; 6: 803-807.
29. Симоненко В.Б. Нейроэндокринные опухоли (клиника, диагностика, лечение).-М.; Издательство «Вооружение. Политика. Конверсия», 2000. –289 с.
30. Левина Л.И. Сердце при эндокринных заболеваниях. – Л.: Медицина, 1989. – 263 с.
31. Трофимов В.М., Краснов Л.М., Шанин С.С. и др. Современные аспекты проблемы хромаффинных опухолей//Российский медицинский журнал.-1992. -№ 5-12. – С.24 – 27.
32. Краснов Л.М. Оценка гемодинамики и эндокринной регуляции кровообращения у больных с гормонально-активными опухолями надпочечников при хирургическом лечении: Автореф. Дис. …к.м.н. –СПб. – 1993. – 24 с.
33. Keating N.L., Cleary P.D., Rossi A.S. Use of hormone replacement therapy by postmenopausal women in the United States//Ann Intern Med 1999; 130:545-53.
34. Лобзин С.В. Вертеброгенные цереброваскулярные расстройства (клинико-патогенетические варианты и дифференцированная терапия). Автореф…д.м.н. СПб., 2001.-45 с.
35. Симоненко В.Б., Тесля А.Н., Широков Е.А., Давыдов О.В. Некоторые особенности течения ишемической болезни сердца в сочетании с вертеброгенными торакалгиями//Клиническая медицина 2007; 1: 61-63.
36. Крылов В.В., Гусев С.А. с соавт. Сосудистый спазм при субарахноидальном кровоизлиянии. Издание второе, исправленное и дополненное. Москва, 2001. – 207 с.
37. Ганжула П.А., Шинкарев С.В. Современные представления о мигрени и лечении мигренозного приступа. Фарматека. 2005; 17: 35-39.
38. Виленский Б.С. Современная тактика борьбы с инсультом. –СПб.: ООО «Издательство ФОЛИАНТ», 2005. – 288 с.
39. Широков Е.А. Нарушения гемостаза/ В кн. Б.С.Виленского «Осложнения инсульта: профилактика и лечение».С-Пб., «Фолиант», 2000. - 94 - 101.
40. Babu A., Kannan C., Mazzone T. Hyperlipidemia and diabetes mellitus/The prevention of stroke/edited by Philip B.Gorelick and M..Alter/The Parthenon Publishing Group, 2002; 17:173-181.
41. Широков Е.А., Леонова С.Ф. Нарушения гемостаза и реологических свойств крови у больных с высоким риском инсульта/Журнал неврологии и психиатрии им. С.С Корсакова. Инсульт: приложение к журналу. Вып. 9. 2003. – С. 140.
42. Gass A., Szabo K., Lanczik O., Hennerici M.G. Magnetic resonance imaging assessment of carotid artery dissection//Cerebrovasc Dis. 2002; 13: 70 – 73.
43. Pace F., Toni D., et al. Spontaneus multiple cervical artery dissection: two case reports and a review of the literature//J Emerg Med.-2004; 27(2): 133-138.
44. Schievink W.I. Spontaneous dissection of the carotid and vertebral arteries//N Engl J Med. 2001; 344: 898 – 906.
45. Albuquerque F.C. Han P.P. et al. Carotid dissection: technical factors affecting endovascular therapy//Can J Neurol Sci. 2002; 29: 54-60.
46. Малышев Н.В., Лунев Д.К., Брагина Л.К., Мусатова И.В. Церебральная гемодинамика при стенозах внутренней сонной артерии // Журн. невропатол. и психиатр. –1987. –N1. – С. 17-23.
47. Широков Е.А., Грудень М.А., Денищук И.С., Елистратова Е.И. Особенности содержания белка S100b и антител к нему в сыворотке крови пациентов при кризовом течении гипертонической болезни //Клиническая медицина. 2006;11: 45 – 48.
Глава из книги "Превентивная кардионеврология". С-Пб, Издательство ФОЛИАНТ, 2008.
